
 Strukturerad
Strukturerad
läkemedels-
information
Återrapportering enligt
E-hälsomyndighetens regleringsbrev 2018
(S2017/07302/RS)
Dnr: 2018/04236
Datum: 2018-12-06

 Förord
Förord
I regleringsbrevet för 2018 har E-hälsomyndigheten fått i uppdrag att färdigställa arbetet
med strukturering av den läkemedelsinformation som ska registreras i nationella
läkemedelslistan.
Denna rapport redovisar hur detta uppdrag har genomförts och vad arbetet resulterat i.
Rapporten är framtagen av senior rådgivare Annika Forsén. Beslut om denna rapport
har fattats av generaldirektören Janna Valik. Senior rådgivare, Annika Forsén, har varit
föredragande.
Janna Valik
Generaldirektör
Stockholm den 6 december 2018
n
tee
ghi
ndy
omsläHe© 4 102
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
2/16
link to page 4 link to page 5 link to page 5 link to page 5 link to page 6 link to page 6 link to page 6 link to page 6 link to page 7 link to page 8 link to page 8 link to page 10 link to page 11 link to page 12 link to page 12 link to page 13 link to page 14 link to page 14 link to page 15 link to page 16

 Innehåll
Sammanfattning ......................................................................................................................... 4
1. Uppdraget ........................................................................................................................... 5
2. Bakgrund............................................................................................................................. 5
3. Genomförande av uppdraget .......................................................................................... 5
3.1 Samverkan .................................................................................................................. 6
4. Resultat ................................................................................................................................ 6
4.1 Läkemedelsinformation ........................................................................................... 6
4.1.1 Förskriven vara, läkemedelsform och styrka ................................................. 6
4.1.2 Aktiv substans .................................................................................................... 7
4.1.3 Dosering .............................................................................................................. 8
4.1.4 Administreringssätt ............................................................................................ 8
4.1.5 Ordinationsorsak och behandlingsändamål ................................................. 10
4.1.6 Läkemedelsbehandlingens längd ................................................................... 11
4.1.7 Senaste datum för när läkemedelsbehandlingen ska följas upp eller avslutas .... 12
4.2 Förvaltning, lagring och distribution av kodverk............................................... 12
4.2.1 Lagring och distribution.................................................................................. 13
4.2.2 Förvaltning av innehåll i kodverk .................................................................. 14
4.3 Nationell informationsstruktur och nationellt fackspråk ................................. 14
4.4 Fortsatt arbete.......................................................................................................... 15
5. Definitioner och förkortningar ..................................................................................... 16
n
Innehåll
Sammanfattning ......................................................................................................................... 4
1. Uppdraget ........................................................................................................................... 5
2. Bakgrund............................................................................................................................. 5
3. Genomförande av uppdraget .......................................................................................... 5
3.1 Samverkan .................................................................................................................. 6
4. Resultat ................................................................................................................................ 6
4.1 Läkemedelsinformation ........................................................................................... 6
4.1.1 Förskriven vara, läkemedelsform och styrka ................................................. 6
4.1.2 Aktiv substans .................................................................................................... 7
4.1.3 Dosering .............................................................................................................. 8
4.1.4 Administreringssätt ............................................................................................ 8
4.1.5 Ordinationsorsak och behandlingsändamål ................................................. 10
4.1.6 Läkemedelsbehandlingens längd ................................................................... 11
4.1.7 Senaste datum för när läkemedelsbehandlingen ska följas upp eller avslutas .... 12
4.2 Förvaltning, lagring och distribution av kodverk............................................... 12
4.2.1 Lagring och distribution.................................................................................. 13
4.2.2 Förvaltning av innehåll i kodverk .................................................................. 14
4.3 Nationell informationsstruktur och nationellt fackspråk ................................. 14
4.4 Fortsatt arbete.......................................................................................................... 15
5. Definitioner och förkortningar ..................................................................................... 16
n
tee
ghi
ndy
omsläHe© 4 102
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
3/16

 Sammanfattning
Sammanfattning
E-hälsomyndigheten har fått i uppdrag att färdigställa arbetet med strukturering av den
läkemedelsinformation som ska registreras i den nationella läkemedelslistan.
Utgångspunkten i arbetet har varit lagen om nationell läkemedelslista som specificerar
vilken information som får lagras i det nya registret.
Sammanfattningsvis har arbetet resulterat i följande:
• Läkemedelsverket kommer att komplettera Nationellt Produktregister för
Läkemedel (NPL) med ”substansens presentationsnamn”. Syftet med denna
information är att i exempelvis användargränssnitt kunna visa vilken substans
ett läkemedel innehåller (avsnitt 4.1.2).
• Arbetet med kravställningen av strukturerad dosering i den nationella
läkemedelslistan är i sin slutfas. En första version av kodverk för
doseringsenhet är framtaget (avsnitt 4.1.3).
• En första version av kodverk för administreringssätt (avsnitt 4.1.4).
• Ett förslag till teknisk lösning för distribution av kodverk är framtagen. Ett
förslag till förvaltning av innehållet i kodverken finns beskriven (avsnitt 4.2).
Förslaget som tagits fram löser det behov som finns i den nationella
läkemedelslistan. Motsvarande behov finns för andra kodverk och på sikt bör
en nationell lösning för förvaltning, lagring och distribution av kodverk hittas.
• Förslag till revideringar och tillägg i Socialstyrelsens termbank. Socialstyrelsen
och E-hälsomyndigheten har beslutat att utgå från en gemensam
begreppsmodell för att harmoniera informationsmodellen som tas fram för
nationella läkemedelslistan och informationsmodellen för läkemedelsordination
som baseras på nationella informationsstrukturen (avsnitt 4.3).
Uppdraget har bedrivits i samverkan med Socialstyrelsen, Läkemedelsverket, Inera och
Sveriges Kommuner och Landsting (SKL). En samverkansgrupp där samtliga aktörer
varit representerade har haft regelbundna möten för att diskutera alla delar av detta
uppdrag och hur arbetet fortskrider. Från denna arbetsgrupp har mindre grupper bildats
för att utreda specifika frågor. Dessa grupper har kompletterats med fler representanter
vid behov, exempelvis personer som arbetar med verksamhetsnära systemförvaltning
inom landstingen. SKL har även i många frågor konsulterat en mindre grupp personer
från landsting och regioner med god kunskap om området.
Nu är arbetet i ett läge där resultatet behöver förankras ytterligare, vilket kommer att ske
i de referensgrupper som E-hälsomyndigheten etablerar inom programmet för
nationella läkemedelslistan.
n
tee
Arbetet kommer att fortsätta under nästa år och till stor del bedrivas inom ordinarie
ghi
ndy
arbete med kravställning och utveckling av den nationella läkemedelslistan.
oms
läHe© 4 102
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
4/16

 1. Uppdraget
1. Uppdraget
Regeringen har i E-hälsomyndighetens regleringsbrev för 2018 givit myndigheten i
uppdrag att färdigställa arbetet med strukturering av läkemedelsinformation som ska
registreras i den nationella läkemedelslistan.
I uppdraget ingår att säkerställa att:
a) den struktur som föreslås för varje informationsmängd bygger på
ändamålsenliga kodverk,
b) informationsmängderna ska vara strukturerade och mappade mot den
nationella informationsstrukturen,
c) den valda struktureringen för varje informationsmängd är förankrad med
representanter för verksamheten,
d) färdiga tekniska lösningar finns för förvaltning av nationella källor,
e) det finns ändamålsenliga tekniska lösningar för hur dessa nationella källor ska
distribueras till hälso- och sjukvårdens vårdsystem.
Uppdraget ska genomföras i samverkan med Socialstyrelsen, Läkemedelsverket och
Sveriges Kommuner och Landsting (SKL), som samtliga har närliggande uppdrag.
2. Bakgrund
I den nationella läkemedelslistan ska informationen vara strukturerad i största möjliga
mån. Det finns flera skäl till detta, vilket utförligt beskrivs i propositionen om nationell
läkemedelslista (prop. 2017/18:223).
E-hälsomyndigheten har i tidigare uppdrag (Strukturerad läkemedelsinformation dnr.
2016/06267) påbörjat arbetet med att strukturera läkemedelsinformationen som ska
registreras i den nationella läkemedelslistan. I det uppdrag som redovisas här ingår att
färdigställa det arbete som påbörjats.
3. Genomförande av uppdraget
Arbetet med strukturerad läkemedelsinformation har på E-hälsomyndigheten skett i
nära samarbete med övrigt kravarbete kopplat till den nationella läkemedelslistan.
Utgångspunkten har varit propositionen om nationell läkemedelslista (prop. 2017/18:
223) och den lagtext som specificerar vilken information om en patients
läkemedelsbehandling som får lagras i registret (3 kap. 8§). Följande information har
n
således ingått i arbetet:
tee
ghi
•
nd
Förskriven vara
y
omslä
• Läkemedelsform
He
©
4 1
•
0
Styrka
2
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
5/16


• Aktiv substans
• Dosering
• Administreringssätt
• Ordinationsorsak och behandlingsändamål
• Läkemedelsbehandlingens längd
• Senaste datum för när läkemedelsbehandlingen ska följas upp eller avslutas
3.1 Samverkan
Arbetet har bedrivits i samverkan med SKL, Inera, Socialstyrelsen och
Läkemedelsverket. En samverkansgrupp där alla aktörer varit representerade har haft
regelbundna möten för att diskutera alla delar av detta uppdrag och hur arbetet
fortskrider. Från denna arbetsgrupp har mindre grupper bildats för att utreda specifika
frågor. Dessa grupper har kompletterats med fler representanter vid behov, exempelvis
personer som arbetar med verksamhetsnära systemförvaltning inom landstingen. SKL
har även i många frågor konsulterat en mindre grupp personer från landsting och
regioner med god kunskap om området.
4. Resultat
Vilken information som får lagras i den nationella läkemedelslistan finns beskrivet i
lagen om nationell läkemedelslista. Utifrån lagtexten har diskussioner förts kring vad
som faktiskt ska dokumenteras vid en ordination och föras över till den nationella
läkemedelslistan. Detta är inte alltid helt entydigt i lagen och den skiljer sig i vissa fall
mot vad som är angivet i Socialstyrelsens föreskrifter och allmänna råd om ordination
och hantering av läkemedel i hälso- och sjukvården (HSLF-FS 2017:37), som styr vad
som ska dokumenteras i journalen vid en läkemedelsordination. Detta gör att arbetet
varit tidskrävande och att det ibland uppstått oenighet kring exakt vad som ska
dokumenteras. Vissa frågor är nu lösta, medan andra kräver ytterligare arbete innan den
slutgiltiga kravställningen på informationen i den nationella läkemedelslistan är klar.
Resultatet av arbetet med de olika informationsmängderna beskrivs i avsnitt 4.1 nedan.
4.1 Läkemedelsinformation
4.1.1 Förskriven vara, läkemedelsform och styrka
n
Parametrarna förskriven vara, läkemedelsform och styrka kommer inte att förändras.
tee
ghi
Även fortsättningsvis ska identiteten för ett läkemedel anges vid överföring av
ndy
information, inte de enskilda parametrarna. Arbete pågår med att förbereda den
omslä
nationella läkemedelslistan för generisk förskrivning och beroende på vilken lösning
He
©
som väljs för detta, blir större eller mindre justeringar i hur ett förskrivet läkemedel
4 102
identifieras aktuella.
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
6/16


 4.1.2 Aktiv substans
4.1.2 Aktiv substans
I den nationella läkemedelslistan finns behov av att på ett tydligt sätt kunna visa vilken
eller vilka substanser en läkemedelsprodukt innehåller i de olika användargränssnitt där
informationen kommer att hanteras. Idag förmedlar Läkemedelsverket information om
vilka substanser en läkemedelsprodukt innehåller ut till vård och apotek via NPL
(Nationellt Produktregister för Läkemedel). Informationen är dock strukturerad på ett
sådant sätt att det inte går att maskinellt få fram den substans som är lämplig att visa i
exempelvis ett användargränssnitt.
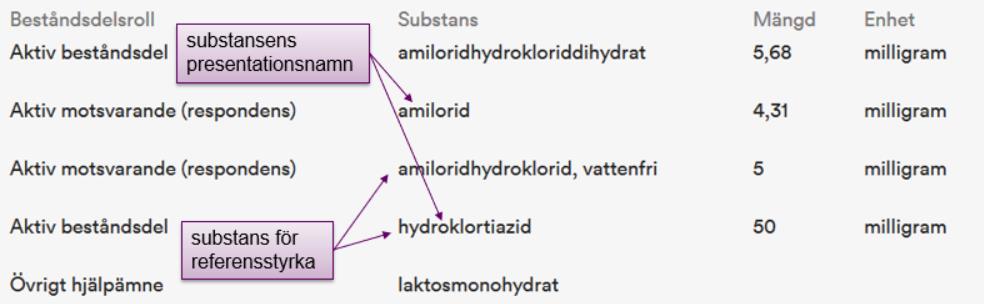
I dialog med Läkemedelsverket har en lösning för detta hittats. Läkemedelsverket
kommer i NPL att markera upp den eller de substanser som är lämpliga som
”substansens presentationsnamn” på respektive läkemedelsprodukt.
Figur 1: Ett exempel på hur de nya flaggorna ”substansens presentationsnamn” och ”substans för
referensstyrka” kommer att anges på en läkemedelsprodukt som har styrkan 5 mg/50 mg.
Denna information förmedlas sedan ut till olika aktörer via E-hälsomyndighetens
system VARA (via Sil för vården) för att användas i de fall man vill visa vilken substans
en läkemedelsprodukt innehåller. Detta är ett led i att öka fokus på substans och stödja
det generiska förhållningssättet. Substansens presentationsnamn är inte lämpligt att
använda vid beräkningar i exempelvis beslutsstöd, i dessa fall behöver man information
om hela sammansättningen av en läkemedelsprodukt. Denna information kommer även
fortsättningsvis finnas med i NPL och distribueras ut via E-hälsomyndighetens system.
Förutom substansens presentationsnamn kommer även substans för referensstyrka att
pekas ut. Substans för referensstyrka är ett begrepp som finns i IDMP (Identification of
Medicinal Products, ISO-standarder för läkemedelsinformation), och avser den substans
som representerar styrkan på läkemedelsprodukten. Denna information efterfrågas
n
tee
bland annat i arbetet med e-recept över landsgränser.
ghi
ndy
När det blir aktuellt att förskriva generiskt så räcker det inte bara med information om
omsläH
substans utan förskrivningarna kommer troligtvis att hanteras med en kombination av
e
©
4
substans, läkemedelsform och styrka. Exakt hur detta ska gå till är ännu inte beslutat. I
102
uppdraget att bygga en nationell läkemedelslista ingår att utforma ett överföringsformat
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
7/16


som möjliggör generisk förskrivning. E-hälsomyndigheten har därför påbörjat en
utredning kring detta.
4.1.3 Dosering
E-hälsomyndigheten har i arbetet med att ta fram en modell för strukturerad dosering
utgått från vårdens doseringsmodell
(Informationsstruktur och enhetlig kortnotation för
dosering, Carelink 2007) och ISO/TS 17251:2016 (Health informatics - Business
requirements for a syntax to exchange structured dose information for medicinal
products). Målet med arbetet är att ta ett första steg från dagens fritextdosering på e-
recepten till en mer strukturerad information. Många journalsystem har redan idag
strukturerad dosering och E-hälsomyndigheten har därför som ambition att utifrån
dessa lösningar hitta en gemensam struktur som kan användas i den nationella
läkemedelslistan.
För att kunna skapa strukturerade doseringar krävs bland annat ett kodverk med
doseringsenheter. En arbetsgrupp med representanter från SKL, Inera, Socialstyrelsen
och tre landsting arbetar med detta, i samband med att kodverk för administreringssätt
tas fram, se avsnitt 4.1.4.
Arbetet med kravställningen för strukturerad dosering i nationella läkemedelslistan är i
sin slutfas. Doseringen är tätt förknippad med administreringssätt (se avsnitt 4.1.4) och
dessa informationsmängder är komplexa och kommer att kräva mycket arbete även
fortsättningsvis, både i utvecklingsarbetet på E-hälsomyndigheten och för de aktörer
som ska ansluta till den nationella läkemedelslistan.
4.1.4 Administreringssätt
I lagen om nationell läkemedelista finns administreringssätt med som en
informationsmängd som får lagras i registret. När man tittar närmare på
administreringssätt så utkristalliserar sig en mer komplex struktur som omfattar flera
parametrar.
Den nationella läkemedelistan ska i möjligaste mån ha informationen strukturerad enligt
de ISO-standarder för läkemedelsinformation, IDMP (Identification of Medicinal
Products), som Läkemedelsverket arbetar med att införa. E-hälsomyndigheten har även
fattat beslut om att använda standarden FHIR (Fast Healthcare Interoperability
Resources) för de externa gränssnitten i nationella läkemedelslistan. I dessa standarder
är informationen om administreringssätt uppdelad i tre kodverk:
• Administreringsväg (ex. oral användning)
• Administreringsmetod (ex. sväljning)
n
tee
•
gh
Administreringsställe (ex. munnen)
i
ndy
För att utreda hur informationen om administreringssätt ska struktureras har två
omsläH
workshopar hållits. Vid dessa tillfällen har samverkansgruppen för strukturerad
e
©
4
läkemedelsinformation kompletterats med kompetens inom Snomed CT samt med
102
representanter från landstingen.
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
8/16


Dessa workshopar har resulterat i behov av ytterligare två kodverk:
• Medicinteknisk produkt för administrering (ex. nebulisator, insulinpump)
• Lokalisation (ex. höger, vänster)
När det gäller källor till dessa kodverk så har kodverken som används i IDMP-
standarderna, som kommer från EDQM (European Directorate for the Quality of
Medicines and Healthcare), utvärderats. För administreringsväg och
administreringsmetod är kodverken från EDQM en källa som fungerar för vården vid
dokumentation av en läkemedelsordination. När det gäller administreringsställe
uppfyller inte EDQM-koderna behoven i vården och det är tydligt att dessa har ett
annat syfte, dvs. att dokumentera en läkemedelsprodukt ur ett regulatoriskt perspektiv.
Fördelen med att använda EDQM-kodverken är att Läkemedelsverket kan ange
administreringsväg och administreringsmetod (via läkemedelsform) på alla
läkemedelsprodukter. Detta gör att förskrivaren utifrån den valda läkemedelsprodukten
kan få förslag på godkänd administreringsväg och administreringsmetod och inte
behöver välja från en lång lista med alla koder.
Läkemedelsverket använder EDQM-koder eftersom det är dessa som används inom det
regulatoriska arbetet i Europa. I diskussionerna kring de nya kodverken i den nationella
läkemedelslistan har behovet av att använda Snomed CT-koder framkommit. Följande
anledningar har lyfts fram:
• Snomed CT är flexibelt och möjliggör anpassningar för nationella behov.
• Hierarkierna i Snomed CT kan stödja ordinatören att välja rätt nivå av
detaljering.
• Snomed CT ger möjlighet att ha synonymer på varje kod, vilket gör att
anpassningar kan göras utifrån specifika behov.
• Det finns i Snomed CT möjlighet att ange en patientvänlig term för varje kod.
Detta innebär att man kan skapa en patientinstruktion (ex. en
doseringsanvisning på en förskrivning) med samma kodverk.
Lösningen blir därför att Läkemedelsverket anger administreringsväg och
administreringsmetod (via läkemedelsform) i NPL. En mappning behöver sedan göras
mellan EDQM-koder och Snomed CT-koder innan informationen distribueras vidare
till vård och apotek. Förslaget är att E-hälsomyndigheten ansvarar för denna mappning i
arbetet med förvaltning av kodverken i den nationella läkemedelslistan (se avsnitt 4.2).
n
tee
ghi
ndy
omsläHe© 4 102
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
9/16


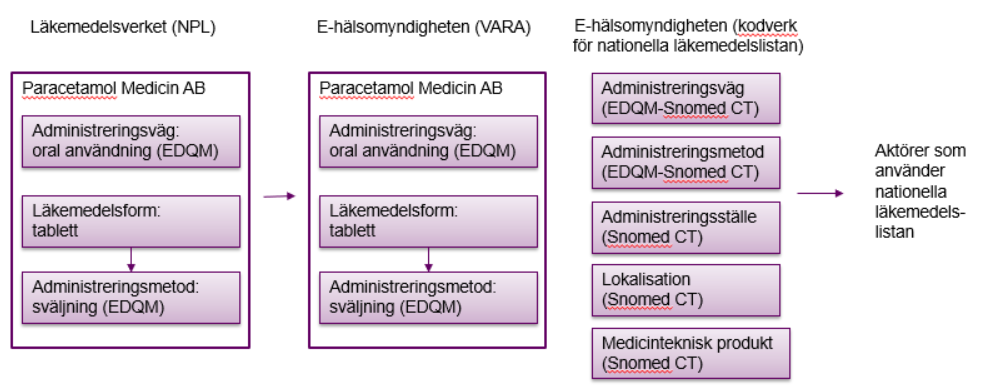 Figur 2: Konceptuell beskrivning av kodverken för administreringssätt i den nationella
Figur 2: Konceptuell beskrivning av kodverken för administreringssätt i den nationella
läkemedelslistan.
En arbetsgrupp med representanter från SKL, Inera, Socialstyrelsen och tre landsting
arbetar med att mappa EDQM-koder till Snomed CT-koder samt att ta fram övriga
kodverk (administreringsställe, medicinteknisk produkt för administrering och
lokalisation). För att få en bild av vilken information som behöver finnas i kodverken så
har SKL samlat in kodverk från ett antal av dagens journalsystem.
Arbetsgruppen har valt att skapa ”rena” kodverk. Exempelvis så delas
administreringsställe (arm, öga, ben osv.) och lokalisation (höger, vänster osv.) upp i två
kodverk istället för att ha ett stort kodverk med höger öga, vänster öga, höger ben,
vänster ben osv. Detta gör att det blir enklare att bygga logik utifrån kodverken, men
det ställer också högre krav på de som bygger användargränssnitt. Användargränssnitten
behöver ha funktioner som underlättar för den som ska mata in informationen så att
man bara behöver ange det som är relevant för den aktuella patienten. Diskussioner
pågår kring att skapa regelverk för hur de olika kodverken ska relatera till varandra som
ett stöd i detta arbete.
De exakta begreppen för dessa fem kodverk är ännu inte beslutade eftersom arbete
pågår med att definiera deras innehåll, vilket behöver göras innan terminologiarbetet
kan slutföras.
De framtagna kodverken behöver underhållas för att vara aktuella och ändamålsenliga.
Detta beskrivs i avsnitt 4.2.2.
4.1.5 Ordinationsorsak och behandlingsändamål
n
I propositionen om nationell läkemedelslista är det specificerat att det är Nationell källa
tee
ghi
för ordinationsorsak som förvaltas av Socialstyrelsen, som ska användas för att
ndy
dokumentera ordinationsorsak och behandlingsändamål. I arbetet med detta uppdrag
omslä
har dessa parametrar främst diskuterats ur ett terminologiskt perspektiv. Resultatet av
He
©
detta arbete har lett till att begreppet ordinationsorsak enligt Socialstyrelsen omfattar
4 102
både behandlingsorsak och ändringsorsak och är att betrakta som en rubrik.
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
10/16


Behandlingsorsak är ett nytt begrepp som avser ”indikation som en ordinatör anger som
skäl till en viss behandling”.
I den nationella läkemedelslistan kommer både behandlingsorsak och ändringsorsak att
finnas med som enskilda parametrar, men även behandlingsändamål (som riktar sig till
patienten).
4.1.6 Läkemedelsbehandlingens längd
I propositionen om nationell läkemedelslista är det inte entydigt beskrivet vad som
avses med läkemedelsbehandlingens längd. I propositionen anges att
läkemedelsbehandlingens längd avser den tid som patienten ska behandlas med ett
läkemedel och att detta i receptsammanhang motsvarar ”behandlingstid”, dvs. den
tidsperiod under vilken en förskriven läkemedelsprodukt ska användas per expediering.
Hur länge en patient ska behandlas med ett läkemedel är dock inte samma sak som
tidsperioden för en expediering. Ett exempel på detta är en blodtrycksbehandling som
pågår tills vidare, men på ett uttag på en förskrivning får man vanligtvis läkemedel som
räcker i tre månader.
Läkemedelsbehandlingens längd kan därmed inte vara samma sak som behandlingstid
utan detta behöver hanteras som två separata informationsmängder.
Behandlingstid
I Läkemedelsverkets föreskrifter om förordnande och utlämnande av läkemedel och
teknisk sprit (HSLF-FS 2016:34) specificeras att mängd läkemedel (förpackningsstorlek)
eller dosering och behandlingstid ska anges på en förskrivning. På elektroniska
förskrivningar anges idag antal av en viss läkemedelsförpackning. I den nationella
läkemedelslistan kommer man troligen att behöva registrera ett pappersrecept innan
man kan göra en expedition på receptet. Farmaceuten kommer då vid registreringen av
pappersreceptet att ange antal läkemedelsförpackningar i enlighet med hur elektroniska
förskrivningar hanteras.
I den nationella läkemedelslistan kommer förskrivningens behandlingstid så som det
avses i Läkemedelsverkets föreskrifter att behövas först när generisk förskrivning blir
aktuell.
Läkemedelsbehandlingens längd
Läkemedelsbehandlingens längd finns idag inte i receptdepån utan skulle bli en ny
informationsmängd i den nationella läkemedelslistan. I dialog med Socialstyrelsen och
n
SKL har det framkommit att läkemedelsbehandlingens längd i Socialstyrelsens
tee
ghi
föreskrifter tolkas som information som hör till ordinationen och inte till förskrivningen
ndy
(men som i vissa fall är relevant att ha med på denna). Ordinationen finns bara i
omslä
journalsystemet och kan sträcka sig över en längre period än förskrivningens giltighet.
He
©
4 102
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
11/16


I första versionen av den nationella läkemedelslistan kommer därför
läkemedelsbehandlingens längd framgå i de fall den anges i doseringen, men inte som
ett eget fält. I doseringen kan förskrivaren exempelvis ange att en kur ska tas i 10 dagar
eller ”ta tabletterna tills smärtan upphör”. Ett annat sätt att förmedla hur länge
läkemedelsbehandlingen ska pågå är att förskrivaren anger ett datum när behandlingen
ska upphöra, vilket i den nationella läkemedelslistan eventuellt kommer att avspeglas i
senaste datum för när läkemedelsbehandlingen ska avslutas, se avsnitt 4.1.7.
4.1.7 Senaste datum för när läkemedelsbehandlingen ska följas upp
eller avslutas
Enligt propositionen för nationella läkemedelslistan är avsikten med att dokumentera
senaste datum för när läkemedelsbehandlingen ska följas upp eller avslutas att
ordinatören varje gång som hen ordinerar ett läkemedel antingen ska välja ett datum för
när läkemedelsbehandlingen ska avslutas eller när den senast ska följas upp.
I Socialstyrelsens föreskrifter och allmänna råd om ordination och hantering av
läkemedel i hälso- och sjukvården (HSLF-FS 2017:37) är dokumentationskraven
uttryckta lite annorlunda. Där står ”när och hur läkemedelsbehandlingen ska följas upp
eller avslutas” (6 kap. 10 §), och inte uttryckt som datum.
I den nationella läkemedelslistan kommer det krävas att förskrivaren anger ett av
datumen, antingen senaste datum för när läkemedelsbehandlingen ska följas upp eller
senaste datum för när läkemedelsbehandlingen ska avslutas. SKL har förmedlat
synpunkter från sina medlemmar om att man ser vissa svårigheter med att ange dessa
datum. Ett problem som lyfts är att det i lagen om nationell läkemedelslista krävs
datum, medan man i journalen (enligt Socialstyrelsens föreskrifter), kan ange när och
hur läkemedelsbehandlingen ska följas upp som en textuell beskrivning, exempelvis
”hör av dig om smärtan inte gått över om tre veckor”. Det finns även funderingar om
hur senaste datum för när läkemedelsbehandlingen ska avslutas bör anges för en
antibiotikakur på 10 dagar, då man inte vet när patienten påbörjar sin behandling.
E-hälsomyndigheten har utifrån dessa synpunkter funderat på hur de två datumen skulle
kunna hanteras i den nationella läkemedelslistan. En tanke är att använda de slutdatum,
alternativt utsättningsdatum, som idag finns i många journalsystem för att fylla i senaste
datum för när läkemedelsbehandlingen ska avslutas i den nationella läkemedelslistan.
Detta behöver diskuteras vidare och E-hälsomyndigheten kommer att ha fortsatt dialog
med myndigheter och vårdrepresentanter innan ett slutgiltigt beslut om hur datumen
ska fungera i den nationella läkemedelslistan kan fattas.
n
tee
gh
4.2 Förvaltning, lagring och distribution av kodverk
i
ndy
Användarna av den nationella läkemedelslistan behöver ha tillgång till ett antal kodverk,
omsläH
exempelvis för administreringssätt (se avsnitt 4.1.4). E-hälsomyndigheten har därför
e
©
4
tagit fram ett förslag på lösning för lagring, distribution och förvaltning av dessa
102
kodverk. Förvaltning behövs bara för de nya kodverk som tas fram i samband med den
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
12/16


nationella läkemedelslistan och inte för exempelvis Nationell källa för ordinationsorsak
(som förvaltas av Socialstyrelsen). Förslaget har presenterats för den strategiska
samverkansgruppen inom E-hälsomyndighetens program för nationella läkemedelslistan
där Socialstyrelsen, SKL, Inera och Läkemedelsverket är representerade. Denna grupp
ska återkomma med eventuella synpunkter på förslaget innan beslut om lösning fattas.
Förslaget som beskrivs nedan löser det behov som finns i den nationella
läkemedelslistan. Motsvarande behov finns för andra kodverk och på sikt bör en
nationell lösning för förvaltning, lagring och distribution av kodverk hittas.
4.2.1 Lagring och distribution
Olika tekniska lösningar har utvärderats för att hitta ett sätt att lagra och distribuera
kodverk i den nationella läkemedelslistan.
Idag tillhandahåller Sil (Svenska informationstjänster för läkemedel) hos Inera ett antal
kodverk för vården. E-hälsomyndigheten kommer att behöva tillhandahålla kodverken
för den nationella läkemedelslistan till alla aktörer (vård, apotek m.fl.) som ska ansluta
till myndighetens tjänster vilket gör att en lösning som tillgodoser detta behov behöver
hittas.
Både Socialstyrelsen och Inera driver projekt som ska ta fram systemstöd för hantering
av kodverk. E-hälsomyndigheten har därför fört dialog med respektive projekt för att
förstå hur deras lösningar kommer att se ut och för att diskutera möjligheter till
samarbete.
Av de olika lösningsförslag som utvärderats så är förslaget att nyttja det externa FHIR-
baserade gränssnittet som E-hälsomyndigheten beslutat om att använda för den
nationella läkemedelslistan. Det innebär att giltiga koder görs tillgängliga i FHIR-
resurser (CodeSystem och ValueSet) så att aktörerna kan använda dessa när man till
exempel skapar en ny förskrivning, ändrar en förskrivning eller liknande. I FHIR-
resurserna anges även en hänvisning till grundkällan så att man kan se ursprunget till
koderna och har möjlighet att läsa in en fullständig en koduppsättning (inte bara urvalet)
om så önskas.
Vissa av de kodverk som tas fram i samband med den nationella läkemedelslistan
kommer att vara användbara även i vårdsystem som inte hanterar förskrivningar. Dessa
system använder inte E-hälsomyndighetens tjänster vilket gör att sådana system kan ha
behov av att hämta kodverken via Sil. Möjlighet finns då att Sil hämtar kodverken från
E-hälsomyndigheten för att inkludera dem i sina tjänster. Nationell källa för
ordinationsorsak är redan på gång att distribueras via Sil för att vara tillgänglig för alla
vårdsystem.
n
För att administrera innehållet i de nya kodverken (inte Nationell källa för
tee
ordinationsorsak) planeras en enkel lösning där justeringar och tillägg kan göras i en fil
ghi
ndy
som sedan valideras och läses in i databasen för den nationella läkemedelslistan på
omsl
E-hälsomyndigheten.
ä
He
©
4
En nationell källa för hantering av kodverk är önskvärd, men fokus har i detta arbete
102
varit att lösa de behov som finns i nationella läkemedelslistan. I och med att det pågår
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
13/16


projekt på exempelvis Socialstyrelsen så kan en nationell kodverkskälla bli aktuell
framöver. Det är då möjligt att anpassa den lösning som nu föreslås för den nationella
läkemedelslistan till den nya källan.
4.2.2 Förvaltning av innehåll i kodverk
Förvaltning av innehållet i kodverken kräver kunskap om både vårdens och apotekens
behov samt om Snomed CT. Detta är delvis frågor som idag inte hanteras i
E-hälsomyndighetens förvaltningsorganisation. Man kan därför tänka sig en lösning där
förvaltning av innehållet ligger hos en annan organisation. Det alternativ
E-hälsomyndigheten anser lämpligast är dock att myndigheten ansvarar för
förvaltningen av de nya kodverk (inte Nationell källa för ordinationsorsak eller de
kodverk som kommer från Läkemedelsverket) och mappningar mellan kodverk som tas
fram för den nationella läkemedelslistan. Förvaltningen behöver ha stöd av en
expertgrupp som har kompetens inom Snomed CT och vårdens behov av information.
Eftersom kodverken kan användas i många olika delar av vården, och inte bara vid
förskrivning, så behöver förvaltningen ha ett vidare perspektiv än bara den nationella
läkemedelslistan.
Även när det gäller förvaltning av innehållet i kodverken kan en framtida nationell
förvaltning av kodverk tänkas överta ansvaret för kodverken, när en sådan finns på
plats.
4.3 Nationell informationsstruktur och nationellt fackspråk
Socialstyrelsen har under 2018 och 2019 i uppdrag att utreda hur termer och begrepp
med koppling till ordination och förskrivning av läkemedel, ska kunna hanteras och
tolkas likartat oberoende av aktör eller system.
Samverkansgruppen för strukturerad läkemedelsinformation har deltagit i arbetet med
termer och begrepp. Resultatet från detta arbete är ett antal förslag till revideringar och
tillägg i termbanken. Fortsatt arbete med förankring och publicering sker nu i enlighet
med Socialstyrelsens terminologiprocess.
E-hälsomyndigheten arbetar med en informationsmodell som beskriver den
information som behövs för att utveckla den nationella läkemedelslistan. Denna modell
är inte helt färdig eftersom kravbilden för nationella läkemedelslistan inte är helt utredd
ännu. Vid arbetet med att ta fram informationsmodellen har dialog förts med
Socialstyrelsen utifrån deras informationsmodell för läkemedelsordination som baseras
på nationella informationsstrukturen (NI). Dialog har även förts med SKL utifrån den
domänmodell för läkemedel som de tagit fram utifrån behov som uttryckts i vården.
E-hälsomyndigheten och Socialstyrelsen har tillsammans beslutat att utgå från en
n
tee
gemensam begreppsmodell och utifrån denna beskriva hur varje begrepp representeras i
ghi
ndy
E-hälsomyndighetens informationsmodell för nationella läkemedelslistan respektive
omsl
Socialstyrelsens informationsmodell för läkemedelsordination som baseras på nationella
ä
He
informationsstrukturen.
©
4 102
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
14/16

 4.4 Fortsatt arbete
4.4 Fortsatt arbete
Arbetet med strukturerad läkemedelsinformation har kommit långt, men frågorna är
komplexa och fortsatt arbete krävs. Vissa frågor är lösta, medan andra kräver ytterligare
utredning innan den slutgiltiga kravställningen på informationen i den nationella
läkemedelslistan är klar. Arbetet som kvarstår kommer att bedrivas i samband med
övrig kravställning och utveckling inom E-hälsomyndighetens program för nationella
läkemedelslistan.
Arbetet är nu i ett läge där resultatet och de krav detta ställer på de verksamheter och
system som ska ansluta till den nationella läkemedelslistan behöver förankras ytterligare.
Förankringen kommer att ske i de referensgrupper som E-hälsomyndigheten etablerar
inom programmet för nationella läkemedelslistan. De diskussioner som uppkommer i
förankringsarbetet kan resultera i behov av justeringar i E-hälsomyndighetens
kravställning på hur läkemedelsinformationen i den nationella läkemedelslistan ska
struktureras.
Arbetet med att skapa FHIR-profiler för gränssnitten i den nationella läkemedelslistan
är en annan faktor som kan påverka strukturen på informationen.
Socialstyrelsen och Läkemedelsverket kommer att ha fortsatta uppdrag under 2019 för
att färdigställa det arbete som behöver göras kopplat till termer, begrepp och
informationsstruktur respektive den nya information som ska införas i NPL. Fortsatt
dialog behövs också med SKL och Inera. E-hälsomyndigheten behöver därför även
under nästa år ha en samordnande roll i de frågor som rör strukturerad
läkemedelsinformation.
n
tee
ghi
ndy
omsläHe© 4 102
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
15/16

 5. Definitioner och förkortningar
Begrepp
Beskrivning
5. Definitioner och förkortningar
Begrepp
Beskrivning
EDQM
European Directorate for the Quality of Medicines and
Healthcare. Organisation som bland annat tillhandahåller
kodverk för läkemedelsinformation, ex. läkemedelsform,
administreringsväg.
IDMP
Fem ISO-standarder, ISO IDMP (Identification of Medicinal
Products) som beskriver den informationsstruktur för läkemedel
som läkemedelsmyndigheter och läkemedelsföretag i Europa ska
använda.
NPL
Nationellt produktregister för läkemedel. Tillhandahålls som en
xml-fil med information om godkända läkemedel,
licensläkemedel och lagerberedningar och tillhörande kodverk.
Förvaltas av Läkemedelsverket.
Snomed CT
Snomed CT är ett internationellt, medicinskt begreppssystem
som är utvecklat för att användas i elektroniska
informationssystem och som är översatt till svenska. Förvaltas i
Sverige av Socialstyrelsen.
Nationell källa
Kodsystem som innehåller behandlingsorsaker och
för
behandlingsändamål. Förvaltas av Socialstyrelsen.
ordinationsorsak
FHIR
FHIR (Fast Healthcare Interoperability Resources) är en
standard framtagen av organisationen HL7. HL7 är en
internationell organisation bestående av experter inom hälso-
och sjukvård som samarbetar för att skapa standarder för
utbyte, hantering och integration av elektronisk
hälsoinformation.
VARA
Det nationella produkt- och artikelregistret för läkemedel samt
de handelsvaror som ingår i förmånen. Förvaltas av
E-hälsomyndigheten.
n
tee
ghi
ndy
omsläHe
©
4 102
uniJ
Dokumentnamn: Strukturerad läkemedelsinformation (S2017_07302_RS)
16/16

































